1/2020


4/2021
Оториноларингология

Аллергический ринит и аллергический конъюнктивит: механизм взаимосвязи и тактика лечения
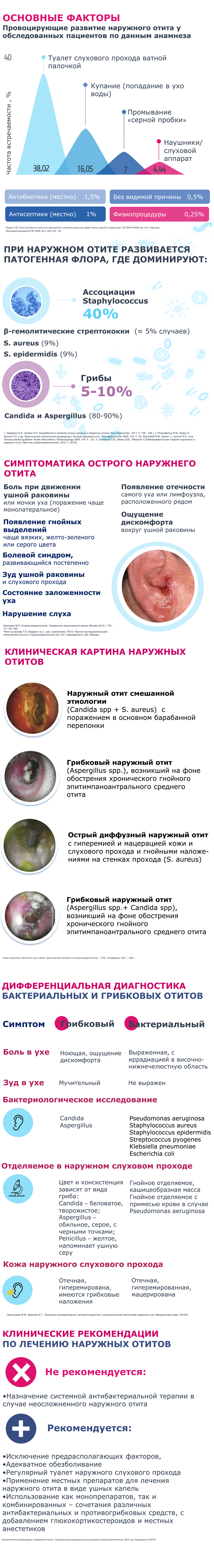
Аллергический ринит (АР) характеризуется воспалением слизистой оболочки полости носа, вызываемым этиологически значимым аллергеном.
Несмотря на то, что при АР внимание обычно сконцентрировано на назальных симптомах, более 80% пациентов испытывают симптомы со стороны глаз.

Аллергический ринит: легко ли выбрать правильное лечение?
Проф. О.М. Курбачева

Трудный пациент
9/2021
Оториноларингология
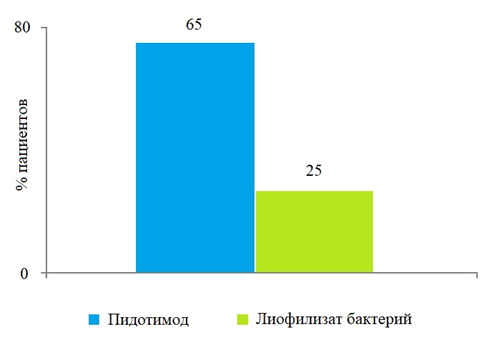
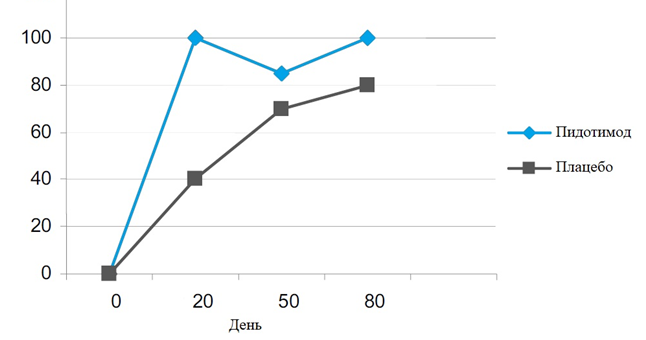
Применение пидотимода у пациентов с хроническим тонзиллитом
Среди заболеваний ЛОР-органов одну из лидирующих позиций занимает хроническая тонзиллярная патология, проявляющаяся хроническим воспалением небных миндалин. Хронический тонзиллит (ХТ) принято считать полиэтиологическим инфекционно-аллергическим заболеванием, возбудителями которого могут выступать стрептококки, стафилококии, гемофильная палочка, лимфотропные вирусы и др [1]. Наиболее частым этиологическим фактором ХТ среди вирусов являются возбудители острых респираторных вирусных инфекций (ОРВИ), включая риновирус, респираторно-синцитиальный вирус, аденовирус и коронавирус.
9-10/2022
Оториноларингология

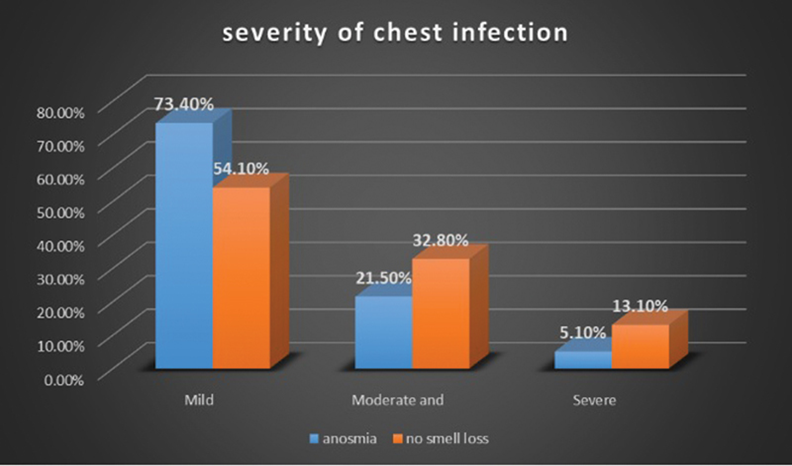
Характер аносмии у пациентов с COVID-19 и ее связь с тяжестью течения болезни. Данные 2023 года
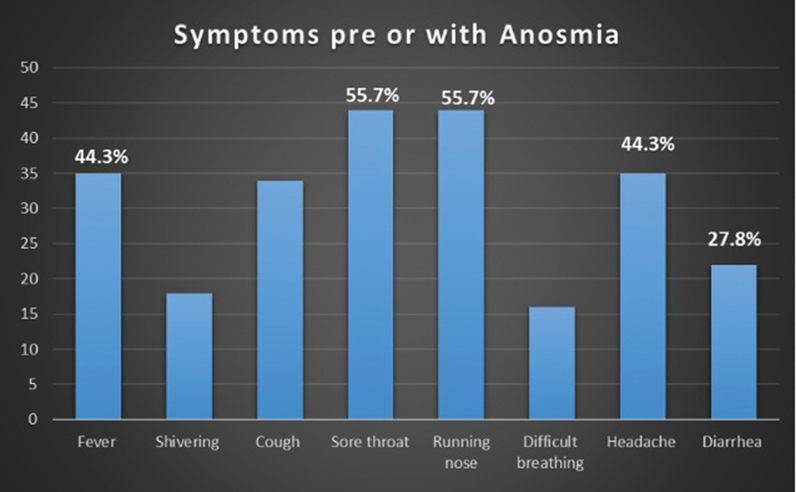
Аносмия является одним из распространенных симптомов COVID-19. Обонятельная дисфункция при коронавирусной инфекции имеет свои особенности, в частности, она протекает в основном без заложенности носа и возникает внезапно на фоне симптоматики, подобной острой респираторной вирусной инфекции. Аносмия у некоторых пациентов с COVID-19 остается стабильной в течение всего периода болезни, а у других может прогрессировать и сочетаться с поражением нижних дыхательных путей.
В 2023 г. в журнале «International Archives of Otorhinolaryngology» опубликована работа, авторы которой определяли критерии гипо- и аносмии у группы пациентов, поступивших с коронавирусной инфекцией, а также изучали связь гипо- и аносмии, тяжести заболевания и соотношения с другими симптомами, чтобы выяснить, существует ли какая-либо корреляция между аносмией и тяжестью инфекционного процесса. Может ли характер гипо- и аносмии стать прогностическим критерием течения COVID-19?

Модифицированная шкала оценки Центора (Centor score) и МакАйзека (McIsaac score)

Международная оценка использования слуховых аппаратов
3/2023
Оториноларингология

Нейросенсорная тугоухость у взрослых
В марте 2023 г. на сайте Минздрава РФ были опубликованы новые клинические рекомендации по нейросенсорной тугоухости у взрослых.
Рассмотрим основные моменты документа.
Нейросенсорная, или сенсоневральная, тугоухость (СНТ) – форма снижения слуха (вплоть до утраты), при которой поражаются какие-либо из участков звуковоспринимающего отдела слухового анализатора, начиная от непосредственно сенсорного аппарата улитки и заканчивая поражением невральных структур.
Согласно статистике, около 6% населения во всем мире (466 млн) имеют нарушения слуха различной этиологии.

Аллергический ринит

Избранные вопросы оториноларингологии

Дифференциальная диагностика острого обструктивного ларингита (крупа) с другими клинически сходными состояниями

7/2024
Оториноларингология

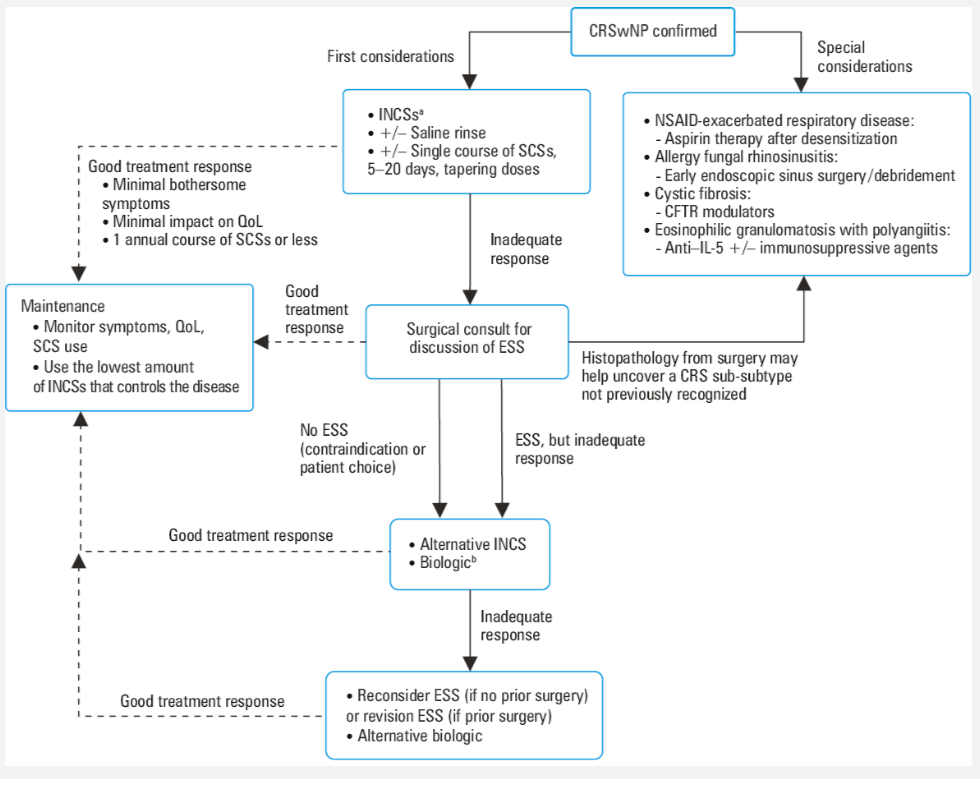
Полипозный риносинусит: дифференцированный подход к ведению пациентов
Полипозный риносинусит (ПРС) – хроническое заболевание слизистой оболочки полости носа и околоносовых пазух (ОНП), характеризующееся образованием и рецидивирующим ростом полипов, состоящих из отечной слизистой оболочки носа.
У детей и подростков ПРС встречается редко. В основном заболевание развивается в возрастной популяции старше 30 лет с преобладанием в возрасте от 50 до 60 лет. У мужчин ПРС встречается чаще. Распространенность ПРС составляет около 5% взрослого населения в мире. В России обращаемость по поводу ПРС зависит от региона: в Санкт-Петербурге распространенность составляет 5,1 на 10 000 человек, а в среднем по стране этот показатель равен 4,9 на 10 000 населения [1].

Первичная цилиарная дискинезия – синдром Картагенера

Раскрыта роль микробиоты околоносовых пазух носа в формировании эозинофильного риносинусита

Ступенчатая терапия ПРС с учетом клинических фенотипов

Чем опасен безобидный назальный вестибулит?

Помимо ингаляций, обильного теплого питья, какой из следующих препаратов показан для начального лечения острого синусита?